「バイオテクノロジーを駆使して、DNAやタンパク質を病気の診断に役立てたい!」
応用生物学部 矢野和義 教授

DNAやタンパク質を応用して、社会に役立てようと研究している矢野先生。現在は、その研究成果を医療分野、特に病気の診断に活かそうと取り組んでいます。今回は、先生の研究室の柱となる3つの研究について、伺いました。
■先生の研究室では、どのようなことに取り組んでいるのですか?
私の研究室では、DNAやタンパク質を使って病気の目印になるものを見つける研究をしています。例えば、抗体のような機能を持つDNAを開発し、病気の診断に応用するという研究があります。DNAというと、生命活動に欠かせないタンパク質をつくるための設計図という捉え方が一般的だと思います。ところが、DNAを構成する4つの物質(ATGC)の配列をうまく変えてあげれば、抗体のように、ある目的の物質にだけくっつく機能を持たせることができるのです。抗体というのは、体内に入った異物を認識し、それだけを捕まえて退治してくれるものです。ただ、どういう配列のDNAにすれば、抗体のように目的とするタンパク質にくっついてくれるかは、よくわかりません。そこで、まずは考え得る、あらゆる配列のDNAをDNA合成機でつくります。そしてそれを認識したいタンパク質にふりかけます。そうすると大半は反応しませんが、もしそこに認識するDNAがあれば、タンパク質と結合したものが見つかります。つまりDNAが抗体のように特定のタンパク質に結合するわけです。その特定のタンパク質に結合する機能を持つDNAのことをDNAアプタマーと呼びます。DNAアプタマーは、すでに広く研究され、利用もされています。そこでこの研究室では、数あるタンパク質の中でもCD4というものに結合するDNAアプタマーをターゲットにして研究しています。このCD4は、エイズ診断の目印となるタンパク質です。今、利用されているエイズ診断薬は、CD4を認識する方法に抗体を用いています。ところが抗体は値段が高く、つくるのに手間がかかるという問題があります。一方、DNAにはそういう心配がほとんどありません。簡単に合成でき、増幅も可能です。ですから今後は、抗体の代わりになるDNAアプタマーが、簡便で低コストなエイズ診断ツールになるのではないかと思って、研究しています。
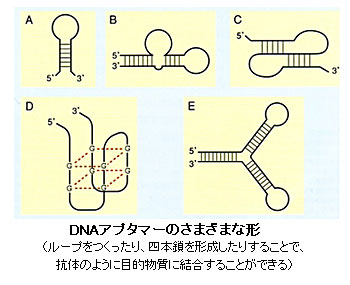
■その研究は、今、どのくらい進んでいるのですか?
5年前から研究を始めて、最初はなかなかうまくCD4と結合するDNAアプタマーが取れなかったのですが、去年、ようやく取れるようになりました。さまざまな角度から試験をした結果、きちんとCD4に結合することが明らかにできています。現在は、本物のヒトの細胞を使って、検証しているところです。CD4は免疫細胞の表面に突起物のように出ているもので、それ自体、免疫反応に非常に重要なものです。エイズウイルスは、その大事なタンパク質であるCD4に結合し、感染します。これまでは、CD4のみを取ってきて、それとDNAを相互作用させるという簡単なシステムで実験してきました。今は、実際に細胞の表面にある状態のCD4に、研究室で発見したDNAアプタマーが結合するかどうかを検証しているところです。ですから研究としては、かなり最終段階に入っていますね。
また、これ以外に、抗体チップの研究や産官学連携で取り組んでいる研究も手がけています。
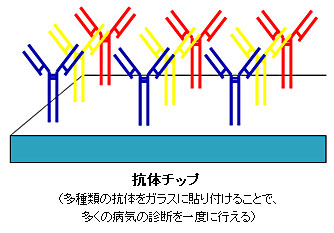
■それは、どのような研究ですか?
抗体チップというのは、スライドガラスに色々な種類の抗体を貼り付けたもののことです。そこに例えば、数滴の血液を落とすだけで、血液中にある病気の目印となるタンパク質が抗体にくっつき、その結合を蛍光シグナルで検出することができます。それを利用すれば、「この人はこういう目印のタンパク質を持っているので、この病気の可能性が高い」と診断できるのです。ただ問題は、病気の目印となるタンパク質は、たいてい濃度が低いということです。ほんの少量しか出てこないタンパク質は光る量も少ないので、現状の抗体チップで見つけることはなかなか難しい。そこでこの研究室では、半導体加工技術という工学的な手法を取り入れて、より高感度にタンパク質を検出する研究をしています。具体的には、スライドガラスのうえにプラズマ重合膜という薄膜と金属膜を製膜することで、たくさん蛍光を光らせることにより、高感度に検出できるチップを開発しました。今のところ、普通の抗体チップの30倍ほど、感度を上げることに成功しています。
また、産官学連携の研究では、「全自動二次元電気泳動装置」の応用に取り組んでいます。簡単に説明すると、さまざまなタンパク質を、それぞれが持つ電気量と分子量の違いという二つのモードで分離する二次元電気泳動という方法があります。この方法を用いると、疾患があるときにだけ出てくる、あるいは消失するタンパク質がわかり、病気の診断に利用できるのです。ところがこの二次元電気泳動は、結果を出すのに20時間以上かかるうえ、作業が煩雑で、しかも再現性が低いので高度な技術を必要とします。ですからお医者さんが片手間に検査するというわけにはいかないのです。そこで、これを全自動化しようと、国、企業、大学とで協力して「全自動二次元電気泳動装置」の開発に乗り出したのです。装置は2007年に完成し、検出時間はわずか1時間40分、しかも全自動ですから学生でも実験結果を出すことができました。今、私の研究室では、この装置を診断にどのように利用できるかを探っているところです。例えば、PC-9細胞株というヒトの肺がんの細胞に、現在使用されている抗がん剤と同じ作用を持つ試薬を投与したものとそうでないものとを、この装置を使って比較しました。その結果、検出されるタンパク質のパターンに違いがあることがわかりました。これはすなわち、この装置を使って薬の効果を目で見て確認できるということになりますので、今後、薬の評価に役立てることができます。また、健康な細胞とがん細胞とを比較することで、がん診断にも役立てることが可能です。

■研究の面白さは、どんなところにありますか?
素材はDNAやタンパク質ですが、結局、それをどう応用するか次第で、色々な機能の高め方があるというところが面白いですね。DNAアプタマーにしても、本来細胞の中にあるDNAは、遺伝子(タンパク質の設計図)としての役割しかないのに、全然違う側面を見せてくれます。それが人の役に立つということであれば、なお面白いです。生物はみんなDNAを持っていますが、生物が思いもしなかった使い方ができるわけですから(笑)。また、先ほど、半導体加工技術を用いている話をしましたが、普通、バイオの研究者はそういう工学的な装置をあまり使いません。でも、そういうちょっと違ったアプローチを加味することで、すごい発見があるというのも面白いものです。そこからオリジナリティが生まれてきますからね。
■最後に今後の展望をお聞かせください。
最初に話したDNAアプタマーの研究と、ふたつめに話した抗体チップの研究を統合させようと思っています。プラズマ重合膜や金属膜を製膜したスライドガラスに、抗体ではなく、さまざまなDNAアプタマーをつけたアプタマーチップをつくりたいのです。これは蛍光シグナルが増強される高感度な基板であるうえ、抗体を使わないので非常に簡便で安価な「高機能性バイオチップ」だと言えます。そこまで発展させるのが夢のひとつですね。さらにプラズマ重合膜の厚さの条件を検討して、感度を数百倍までもっていければうれしいです。
[2010年10月取材]
■応用生体科学(矢野和義)研究室
https://www.teu.ac.jp/info/lab/project/bio_dep/104.html
・次回は12月10日に配信予定です。
2010年11月12日掲出


