血糖値センサーチップ用の耐熱性と長期安定性に優れた酵素を発見

東京工科大学(東京都八王子市片倉町、学長:軽部征夫)応用生物学部の横山憲二教授らの研究グループは、好熱性糸状菌から耐熱性と長期安定性に優れたグルコース脱水素酵素(GDH)を発見しました。
今後、糖尿病患者が自宅などで使用する血糖値センサーに用いられる酵素としての応用が期待されます。
国立研究開発法人産業技術総合研究所との共同研究(注1)によるもので、本研究成果は、2017年1月1日に科学誌「Applied Microbiology and Biotechnology」に掲載されました(注2)。
【背景】
厚生労働省の統計(注3)によると、国内の糖尿病が強く疑われる人は950万人、糖尿病の可能性を否定できない人は1,100万人と推定されています。
中でも、インスリンの自己注射療法を行っている糖尿病患者は、自己血糖値センサーによる日常的な血糖値管理が有効とされています。このセンサー素子として、これまでグルコースオキシダーゼや、酸素の影響を受けないピロロキノリンキノン依存型GDH、さらに点滴の成分の影響を受けないフラビンアデニンジヌクレオチド依存型GDH(FAD-GDH)が利用されてきました。
しかし、これらの酵素を利用した血糖値センサーは、高温での使用、常温での長期保存が困難でした。
【成果】
FAD-GDHは、FADを補因子としてグルコースからD-グルコノ-1,5-ラクトンへの酸化反応を触媒する酵素であり、いくつかの常温性糸状菌から発見されています。
本研究では、これらよりも耐熱性と長期安定性に優れたFAD-GDHの取得を目的として、好熱性糸状菌から同酵素の遺伝子のスクリーニングを行い、大腸菌と酵母を用いて作製を試みました。
具体的には、32株の好熱性糸状菌に対して、Aspergillus属FAD-GDH遺伝子に基づいて設計した縮重プライマーを用いて、ゲノムDNAを鋳型とする縮重PCRを行いました(注4)。
その結果、複数の株に対して、FAD-GDH遺伝子と高い相同性を有する遺伝子断片の増幅を確認しました。この遺伝子断片をプローブとしてFAD-GDH全領域を包括するゲノムDNAをクローニングし、この遺伝子がコードするタンパク質を大腸菌と酵母で発現させました。その結果、好熱性糸状菌Talaromyces emersonii、Thermoascus crustaceus由来タンパク質は、分泌シグナル配列を除去することにより、可溶性画分から精製することができました。これらのタンパク質の吸収スペクトルを測定すると、FADに特徴的な380nmと450nm付近に二つのピークが観察され、グルコースを添加するとこれらの吸収が消失することから、グルコースを基質としFADを補因子とする酵素FAD-GDHであることが示唆されました。また、このFAD-GDHは、基質特異性に優れており、常温性Aspergillus oryzae FAD-GDHよりも高い熱安定性を示しました。
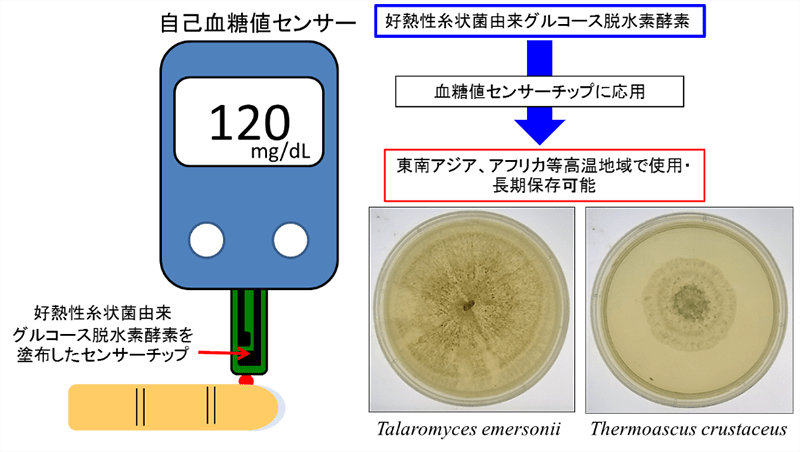
図1 好熱性糸状菌グルコース脱水素酵素を用いた自己血糖値センサー概念図
糖尿病患者が自宅等で使用する自己血糖値センサーの酵素として使用するグルコース脱水素酵素を好熱性糸状菌から発見しました。東南アジア、アフリカ等の高温地域で使用、長期保存の可能性が広がります。
【社会的・学術的なポイント】
新たに発見した酵素は、耐熱性に優れ長期保存できる血糖値センサーチップに利用できると期待されます(図1)。
特に東南アジア、インド、アフリカといった高温地域においても利用可能と思われます。
今後は、さらに活性と安定性の高い酵素を目指すとともに、本酵素を使用した血糖値センサーの製品化に向けて研究開発を進めます。
(注1)共同研究者:国立研究開発法人産業技術総合研究所ナノ材料研究部門 平塚淳典主任研究員
(注2)著者:Kazumichi Ozawa, Hisanori Iwasa, Noriko Sasaki, Nao Kinoshita, Atsunori Hiratsuka, and Kenji Yokoyama, 論文名:Identification and characterization of thermostable glucose dehydrogenases from thermophilic filamentous fungi, 雑誌:Applied Microbiology and Biotechnology, Volume 101, Issue 1, Page 173-183, 2017.
(注3)厚生労働省「平成24年国民健康・栄養調査」
(注4)縮重プライマー/縮重PCR:タンパク質のアミノ酸配列から未知の遺伝子を取得する場合、一種類のアミノ酸に対して複数のコドンが存在するため、アミノ酸配列から推定される塩基配列は複数の可能性がある。そのため、アミノ酸配列から未知の遺伝子を取得する目的で設計されるプライマーを「縮重プライマー」と言い、それを使ったポリメラーゼ連鎖反応(Polymerase Chain Reaction、PCR)を「縮重PCR」と言う。
■東京工科大学応用生物学部 横山憲二(応用生化学)研究室
「健康を測る、健康を創る」ためのヘルスケア工学に関する研究を行っている。
[主な研究テーマ]
1.がんマーカー等の疾患関連タンパク質を高速全自動で分離・解析する装置の開発
2.糖尿病患者が使用する血糖値センサーとそれに利用される酵素に関する研究
3.血液透析装置の高機能化に関する研究
4.食品有用成分の電気化学分析
5.イオン液体中の酵素反応
6.連続測定型血糖値センサーに関する研究
【研究内容に関しての報道機関からのお問い合わせ先】
東京工科大学 応用生物学部 教授 横山憲二
Tel:042-637-2419(研究室直通)
E-mail:yokoyamakj(at)stf.teu.ac.jp
※atはアットマークに置き換えてください。


